Arthrite : le rôle primordial du kinésithérapeute

Cette année, la Journée de la kinésithérapie est consacrée à l’arthrite. C’est l’occasion de faire le point sur le rôle primordial joué par le kinésithérapeute dans la prise en charge de cette maladie.
Le kinésithérapeute, maillon essentiel pour améliorer la qualité de vie des patients souffrant d’arthrite
|
| Résumé | |
|---|---|
|
Introduction
Les rhumatismes inflammatoires sont une des principales causes d’invalidité dans notre pays. On considère que 200.000 personnes souffrent de ces affections en Belgique. On distingue les rhumatismes mécaniques dégénératifs des rhumatismes inflammatoires, caractérisés par de l’arthrite qui peut toucher les articulations périphériques et la colonne. Les rhumatismes inflammatoires comprennent également les maladies métaboliques avec des dépôts, dont la plus fréquente est la goutte. Parmi les affections se présentant par des arthrites périphériques, on distingue la polyarthrite rhumatoïde (PR), les spondyloarthropathies séronégatives comprenant l’arthrite psoriasique, la spondylarthrite ankylosante et les rhumatismes inflammatoires systémiques dont le lupus et la sclérodermie. La PR est une des maladies inflammatoires chroniques les plus fréquentes (1). Elle touche 0,5 à 1% de la population avec un sex-ratio de 3 femmes pour 1 homme. Elle peut survenir à tout âge mais préférentiellement après la grossesse ou la ménopause. Elle atteint en priorité les articulations, principalement les mains et les pieds, mais peut être à l’origine d’une atteinte pulmonaire, oculaire, de nodules rhumatoïdes et d’un risque cardio-vasculaire augmenté.
Elle peut entrainer un handicap fonctionnel majeur, une altération de la qualité de vie et avoir des conséquences socio-économiques non négligeables (1,2,3).
Il est donc primordial pour réduire les dommages irréversibles de poser le diagnostic de manière précoce et de débuter un traitement le plus rapidement possible. En effet, la littérature évoque à ce propos une « fenêtre d’opportunité » durant laquelle le fait de débuter le traitement améliore la qualité de vie à long terme (4,5,6). Cet article illustre les derniers développements et l’intérêt de la kinésithérapie dans le cadre de la PR, qui peuvent s’appliquer aux autres polyarthrites.
Prise en charge de l’arthrite
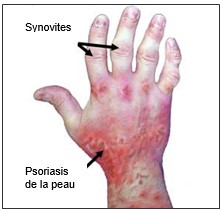
La reconnaissance de toute arthrite inflammatoire débutante est essentielle. L’anamnèse et l’examen clinique sont les piliers essentiels afin de distinguer les différentes formes d’arthrites inflammatoires des atteintes métaboliques liées aux dépôts dans les articulations ou des atteintes mécaniques liées à l’usure du cartilage. Les antécédents familiaux seront également pris en compte, car ils représentent une augmentation du risque chez certains patients. La présentation clinique est très hétérogène, ce qui permet de distinguer les formes classées dans les PR ou les spondyloarthropathies séronégatives avec des atteintes oligoarticulaires, des dactylites ou des formes associées à des enthésopathies inflammatoires. L’atteinte typique de la PR associe des douleurs et des gonflements articulaires bilatéraux et symétriques, d’apparition récente, avec une raideur matinale et des résurgences algiques nocturnes (1,5,7). Les articulations les plus souvent atteintes sont les mains et les pieds (5,7).
Un petit nombre de patients (5%) peut également entrer dans la maladie par une atteinte rhizomélique, intéressant alors plutôt les épaules et les hanches.
Le patient peut rarement débuter la maladie par des plaintes extra-articulaires : atteinte pulmonaire, oculaire ou nodules rhumatoïdes (1,5,7).
 |
L’évaluation clinique minutieuse est essentielle à la recherche des signes de synovite et de ténosynovite périphériques. Il est recommandé de faire un compte articulaire en notant les articulations douloureuses et gonflées.
|
|
Ce bilan de base peut être enrichi par la réalisation d’une échographie articulaire, qui permet de détecter de manière précoce les synovites, ténosynovites et érosions, ou d’une IRM qui pourra mettre en évidence toutes ces lésions précoces et l’œdème osseux (zone de développement potentiel d’érosions) (1). Ces examens sont en effet plus sensibles pour détecter l’arthrite débutante, mais leurs interprétations devront être prudentes car les synovites a minima peuvent être influencées par des facteurs mécaniques, métaboliques et l’âge.
|
|

Les rhumatologues ont développé ces dernières années des outils cliniques et paracliniques très utiles pour évaluer l’arthrite et la PR. Ils permettent de mesurer de manière plus précise l’activité de la maladie et la réponse thérapeutique. La première démarche, une fois le diagnostic de PR confirmé, sera de compter les articulations douloureuses et gonflées par un examen minutieux des différents sites articulaires. Il sera également demandé au malade de compléter un questionnaire évaluant sur une échelle analogique de 0 à 10 le degré d’activité de la maladie, de la douleur, de la fatigue et de répondre à des questions évaluant le degré de difficultés de réaliser des activités courantes (questionnaire HAQ).
L’intégration du nombre d’articulations douloureuses, gonflées, de l’activité de la maladie évaluée par le patient et du taux inflammatoire (CRP ou VS), permet de calculer un score composite d’activité de la maladie (score DAS, le plus utilisé étant le DAS28-CRP en se limitant aux articulations des membres supérieurs et des genoux). Ce score validé dans de nombreux essais cliniques (8) permet à la fois de définir le degré d’activité (importante, modérée, légère ou rémission) et permet d’évaluer de manière plus précise la réponse thérapeutique. Ce score reste cependant imparfait, car il inclut des paramètres subjectifs comme le compte articulaire douloureux et l’évaluation de la maladie par le malade ; il doit dès lors faire l’objet d’une interprétation et d’une analyse des composantes objectives et subjectives du score DAS (7).

D’autres scores ont été développés pour évaluer l’activité de la maladie comme le SDAI (Simplified Disease Activity Index) et le CDAI (Clinical Disease Activity Index) (8). Ce dernier est facile à réaliser car il consiste en une simple addition des articulations douloureuses et gonflées, de l’activité de la maladie évaluée par le patient mais également par le médecin (7). Le SDAI prend en compte la CRP en plus des éléments précités et constitue donc le score le plus global.
Les radiographies des mains et des pieds seront répétées annuellement (1) lors des 5 premières années afin de s’assurer de l’absence de destruction progressive. Les différents paramètres radiologiques de la PR sont le gonflement des tissus mous, l’ostéoporose périarticulaire, les érosions, le pincement de l’articulation, le désalignement, les subluxations, l’ankylose et la formation de kystes intraosseux. Afin de définir l’évolution, divers scores sont proposés dans la littérature, dont le plus validé est le score de Sharp Van der Heijde (9).
La prise en charge doit également inclure une évaluation des atteintes extra-articulaires et des maladies associées, comprenant principalement les maladies cardiovasculaires dont le risque est majoré dans la PR et l’arthrite psoriasique. Chaque malade bénéficiera, lorsque la maladie est contrôlée sur le plan inflammatoire, d’une évaluation de ses capacités physiques et un bilan fonctionnel. Enfin, des programmes d’information et d’éducation sur la maladie seront proposés car on sait que la compréhension et l’adhésion thérapeutique sont des facteurs clés pour la compliance thérapeutique et la réponse clinique.
La littérature récente nous indique qu’une prise en charge précoce et intensive permet de modifier l’évolution de l’arthrite et de la PR (10,11). La rémission, ou si elle n’est pas possible une activité faible de la maladie, doivent être l’objectif à atteindre (10,11). L’inflammation est la cible thérapeutique principale (1). En réduisant l’inflammation rapidement, nous pouvons prévenir les dommages articulaires irréversibles et améliorer la fonction physique du patient à long terme (10).
La première médication pendant la phase de diagnostic et d’évaluation repose sur un traitement symptomatique, par exemple par AINS (5) ou antalgiques, en évitant les corticostéroïdes pour ne pas masquer la maladie.
Une fois le diagnostic établi, un traitement de fond par un sDMARD (synthetic Disease-Modifying Antirheumatic Drug), idéalement le méthotrexate, sera débuté (3,7). En cas d’échec après 3 à 6 mois d’évaluation, le méthotrexate pourra être associé ou remplacé par d’autres traitements de fond tels que la sulfasalazine, l’hydroxychloroquine ou le leflunomide (12). Si une activité élevée de la maladie persiste malgré les sDMARDs, les patients peuvent bénéficier d’un traitement par bDMARDS (Biologic Disease-modifying Antirheumatic Drug) ou par un inhibiteur des JAK kinases (2,12). L’indication d’un bDMARD est indispensable chez les patients réfractaires au sDMARDs avec des facteurs de mauvais pronostics (facteur rhumatoïde ou ACPA positifs et lésions radiologiques notamment) Ces traitements ont pu être développés suite à une meilleure compréhension de l’activation du système immunitaire, en bloquant certaines protéines inflammatoires (TNF, IL-6..) ou en modulant les lymphocytes (T ou B). Les critères utilisés en Belgique sont une maladie active (DAS28-CRP > 3.7) malgré l’utilisation de 2 sDMARDs. Il existe actuellement 4 types de bDMARDS avec des mécanismes d’action différents (1) :
- Agents bloquant le TNF (infliximab, adalimumab, certolizumab, etanercept et golimumab).
- Agents bloquant la co-stimulation avec le lymphocyte T (abatacept).
- Agents bloquant le récepteur de l’IL6 (tocilizumab, saralimumab).
- Agents inhibant les lymphocytes B (rituximab).
On dispose également de biosimilaires pour certaines de ces molécules. Les biosimilaires sont des molécules pharmaceutiques qui sont hautement similaires aux traitements biologiques déjà approuvés (2). Les inhibiteurs des JAK kinases sont les dernières molécules arrivées sur le marché. Ce ne sont pas des traitements biologiques mais des molécules orales synthétiques ciblées permettant de moduler la voie enzymatique intracellulaire de la production des cytokines pro inflammatoires. Nous disposons des molécules suivantes en Belgique : tofacitinib, baricitinib, upadacitinib et filgotinib.
Le principal obstacle à l’utilisation des biothérapies en clinique est leur coût élevé par rapport aux DMARDs conventionnels : un traitement d’une année représente un coût de 10.000 à 15.000 €. À l’opposé, il faut prendre en considération les économies réalisables grâce à l’introduction précoce des traitements biologiques, avec une réduction des frais médicaux à long terme d’une maladie chronique par la prévention du handicap fonctionnel, des maladies associées et de la préservation de la vie socioprofessionnelle. Des études cliniques ont démontré que l’utilisation précoce de ces agents chez des patients présentant une PR débutante apporte un bénéfice surtout marqué sur la prévention des destructions articulaires (11).
Outre les traitements médicamenteux, la prise en charge de la polyarthrite rhumatoïde doit être multidisciplinaire.
L’infirmière qui permettra la coordination, le suivi et l’éducation thérapeutique.
Le kinésithérapeute effectuera le bilan fonctionnel, l’éducation et la prise en charge souvent indispensable dans les formes évoluées.
L’ergothérapeute aura comme objectif de lutter contre les déformations des doigts, d’éduquer le patient (hygiène gestuelle et de vie) et de lui donner des conseils.
Le chirurgien dont l’intervention est nécessaire pour les arthroplasties et pour corriger les déformations dans certains cas avancés.
Le psychologue est souvent nécessaire pour soutenir le patient dans sa maladie.
L’assistant social apportera son aide en vue de maintenir ou d'adapter les capacités professionnelles du patient.
Prise en charge par le kinésithérapeute de l’arthrite
La kinésithérapie est une part essentielle de la prise en charge en cas de polyarthrite rhumatoïde, d’arthrite psoriasique et surtout de spondylarthrite ankylosante (forme axiale). Elle doit être préventive et curative, la prise en charge se fera principalement en dehors des phases inflammatoires. L’objectif est que le patient soit placé dans un contexte favorisant la compréhension et la prise en charge de sa maladie, son traitement, ainsi que les moyens de prévention afin de maintenir sa condition physique et pour éviter les déformations. Le but principal de la rééducation elle-même est de limiter les conséquences fonctionnelles des poussées. La première étape est de communiquer par le rhumatologue l’évaluation de la polyarthrite avec les différents scores cliniques (DAS), fonctionnels (HAQ), l’atteinte radiologique, les maladies associées de chaque malade souffrant de PR. Le kinésithérapeute réalisera ensuite un bilan fonctionnel des articulations et de la condition physique. Le malade sera également interrogé par rapport à ses souhaits, sa motivation ou ses craintes par rapport à l’activité physique, ce que l’on appelle la kinésiophobie. Pour que les séances se passent bien, elles doivent être adaptées aux capacités et aux symptômes de chaque patient, c’est-à-dire notamment ne pas provoquer de douleurs, et rester relativement courtes avec de nombreuses pauses. Le programme de soins est flexible et s’adapte aux nouvelles lésions possibles. Plusieurs objectifs sont poursuivis (voir le tableau ci-dessous) :
- Pendant les phases inflammatoires, l’idée est de réduire les douleurs et de reposer les articulations, dans la position la plus fonctionnelle tolérée.
- Hors des phases inflammatoires, on se concentre surtout sur la diminution des contraintes et des facteurs de déformation, la stabilité articulaire et la prise de conscience des gestes nocifs.
Les principales techniques employées sont les suivantes :
- Des mobilisations douces, actives aidées selon les amplitudes tolérées, pour prévenir les déformations.
- Des postures douces générales.
- Des exercices d’entretien musculaire.
- Des massage décontracturants (en dehors des poussées douloureuses).
- Des postures antalgiques (attelles de nuit).
- L’apprentissage d’un programme d’entretien à domicile.
- Un travail fonctionnel.
- Des techniques de contraction musculaire.
- De la cryothérapie et/ou de l’électrothérapie antalgique.
- Réentraînement cardio-respiratoire.
- Renforcement musculaire.
- Education du patient : reprise d’une activité physique d’entretien.
Avant de démarrer les soins proprement dits, le kinésithérapeute se concerte avec le rhumatologue et procède à un bilan de la douleur, ainsi qu’à un examen minutieux de chaque articulation. Cela permet de savoir dans quelle phase de la maladie se situe le patient (évolution, fin d’évolution, poussée…) et de choisir les techniques les plus adaptées. Le soutien moral et psychologique est un aspect important de l’accompagnement, c’est pourquoi le kinésithérapeute peut aussi orienter la personne vers des associations de malades.
Tableau de suivi de la PR pour la kinésithérapie (14)
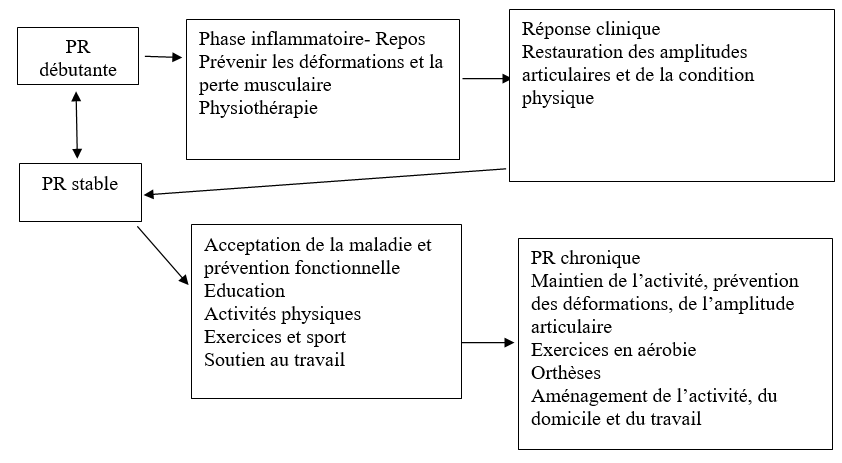
Au début de la maladie, il est conseillé de maintenir une activité physique qui préserve les articulations. Ces mesures sont complétées par un programme de rééducation fonctionnelle. Mises en place dès le début de la maladie, les différentes techniques de rééducation fonctionnelle vont permettre au patient de préserver sa mobilité et son autonomie, et prévenir les déformations articulaires. Dans certains cas, un traitement chirurgical est nécessaire pour augmenter la mobilité d’une articulation ou la stabiliser. La rééducation doit être proposée le plus tôt possible car il est plus facile de prévenir une déformation ou une raideur que de la corriger. Les objectifs de la rééducation sont de soulager la douleur, de prévenir les déformations articulaires et de maintenir l’autonomie et la qualité de vie. C’est une rééducation globale qui concerne toutes les articulations et qui est éventuellement associée à des massages contre les douleurs ou les contractures.
 Depuis l’apparition des traitements biologiques et l’amélioration du taux de rémission, la place de la rééducation dans la prise en charge de la polyarthrite rhumatoïde est moins importante, mais elle reste utile à tous les stades de la maladie, en complément des autres traitements. Lors de poussée inflammatoire, il peut être intéressant de pratiquer des applications de froid sur les articulations touchées (toujours à travers un linge humide et pour une durée inférieure à vingt minutes pour éviter de brûler la peau). En dehors des poussées, l’application de chaleur est bénéfique et facilite la rééducation (boues chaudes ou fangothérapie). La kinébalnéothérapie consiste à faire travailler les articulations et les muscles dans un bassin chauffé (environ 35° C). Elle est généralement utile et bien tolérée, mais elle est contre-indiquée en période de poussée inflammatoire. La kinébalnéothérapie permet la décontraction musculaire, l'augmentation de la flexibilité articulaire et la marche, même chez les personnes qui souffrent de polyarthrite rhumatoïde sévère au niveau des hanches et des genoux.
Depuis l’apparition des traitements biologiques et l’amélioration du taux de rémission, la place de la rééducation dans la prise en charge de la polyarthrite rhumatoïde est moins importante, mais elle reste utile à tous les stades de la maladie, en complément des autres traitements. Lors de poussée inflammatoire, il peut être intéressant de pratiquer des applications de froid sur les articulations touchées (toujours à travers un linge humide et pour une durée inférieure à vingt minutes pour éviter de brûler la peau). En dehors des poussées, l’application de chaleur est bénéfique et facilite la rééducation (boues chaudes ou fangothérapie). La kinébalnéothérapie consiste à faire travailler les articulations et les muscles dans un bassin chauffé (environ 35° C). Elle est généralement utile et bien tolérée, mais elle est contre-indiquée en période de poussée inflammatoire. La kinébalnéothérapie permet la décontraction musculaire, l'augmentation de la flexibilité articulaire et la marche, même chez les personnes qui souffrent de polyarthrite rhumatoïde sévère au niveau des hanches et des genoux.
L’ergothérapie consiste à apprendre au patient à préserver son autonomie en dépit du handicap, en adaptant ses gestes et son environnement. Elle est nécessaire dès le début de la maladie et permet la confection des orthèses de main (voir ci-dessous), le choix des aides techniques (par exemple des outils adaptés, des objets à gros manche, etc.) et l’adaptation des lieux de vie et professionnels. Utilisés précocement, les appareillages permettent de prévenir les déformations articulaires : orthèses de repos (pour les mains), orthèses de correction (orthèses plantaires et chaussures orthopédiques). Ces appareillages peuvent être intéressants pour diminuer la douleur et prévenir certaines déformations des articulations. Confectionnés sur mesure dès le début de la maladie par les kinésithérapeutes ou les ergothérapeutes et réalisés selon des normes techniques rigoureuses, ils sont portés pendant la nuit et, si possible, pendant quelques heures dans la journée, surtout au moment des poussées. Des appareillages de travail sont également utilisés pour réduire les déformations des doigts.
La prise en charge de la kinésithérapie est en constante évolution et profite d’une prise en charge thérapeutique plus efficace de la PR débutante et des formes chroniques. De nombreux malades sont en rémission, n’ont ni atteinte radiologique ni déformation. Ceci permet de développer des programmes de plus grandes intensités avec exercice d’endurance et de renforcement musculaire. Ces programmes doivent être acceptés par l’ensemble des intervenants (patients, rhumatologues et kinésithérapeute) et ont un impact très positif sur l’endurance cardiorespiratoire, la prévention du surrisque cardiovasculaire de l’arthrite chronique et du syndrome métabolique.
La rééducation est également essentielle pour améliorer de nombreuses problématiques de l’arthrite chronique telles que la fatigue, la douleur chronique, les troubles anxieux, dépressifs, les problèmes de sommeil et l’ostéoporose.
Ces 2 schémas illustrent en pratique ce que nous proposons à nos malades.

Conclusion
La connaissance plus précise de l’arthrite, une meilleure évaluation clinique, l’avènement de nouveaux traitements plus efficaces et la prise en charge par le kinésithérapeute ont permis de changer l’évolution de la polyarthrite. Les stratégies thérapeutiques multidisciplinaires ont comme objectifs principaux la rémission, la prévention du handicap et la restauration d’une qualité de vie personnelle, familiale, sociale et professionnelle normale. Le travail en équipe et la prise en charge complémentaire par le kinésithérapeute sont dès lors essentiels pour prévenir les conséquences potentielles et irréversibles de ces maladies.
Références
- Smolen JS, Aletaha D, McInnes. Rheumatoid arthritis. Lancet. 2016 Oct22;388(10055):2023-2038.
- Burmester GR, Pope JE. Novel treatment strategies in rheumatoid arthritis. Lancet. 2017 Jun 10;389(10086):2338-2348.
- Bortoluzzi A, Furini F, Generali E, Silvagni E, Luciano N, Scirè CA. One year in review 2018: novelties in the treatment of rheumatoid arthritis. Clin Exp Rheumatol. 2018 May-Jun;36(3):347-361.
- Nam JL. Rheumatoid arthritis management of early disease. Curr Opin Rheumatol. 2016 May;28(3):267-74.
- Littlejohn EA, Monrad SU. Early Diagnosis and Treatment of Rheumatoid Arthritis. Prim Care. 2018 Jun;45(2):237-255.
- Verhoeven MMA, Welsing PMJ, Bijlsma JWJ, van Laar JM, Lafeber FPJG, Tekstra J, Jacobs JWG. Effectiveness of Remission Induction Strategies for Early Rheumatoid Arthritis: a Systematic Literature Review. Curr Rheumatol Rep. 2019 Apr23;21(6):24.
- Aletaha D, Smolen JS. Diagnosis and Management of Rheumatoid Arthritis: A Review. JAMA. 2018 Oct 2;320(13):1360-1372.
- Mian A, Ibrahim F, Scott DL. A systematic review of guidelines for managing rheumatoid arthritis. BMC Rheumatol. 2019 Oct 22;3:42.
- van der Heijde D. How to read radiographs according to the Sharp/van der Heijde method. The Journal of rheumatology. 2000 ;27(1) :261-3.
- Ajeganova S, Huizinga T. Sustained remission in rheumatoid arthritis: latest evidence and clinical considerations. Ther Adv Musculoskelet Dis. 2017 Oct;9(10):249-262.
- Legrand J, Kirchgesner T, Sokolova T, Vande Berg B, Durez P: Early clinical response and long-term radiographic progression in recent-onset rheumatoid arthritis: Clinical remission within six months remains the treatment target. Joint Bone Spine. 2019 Oct; 86(5):594-599.
- Smolen JS, Landewé R, Bijlsma J, Burmester G, Chatzidionysiou K, Dougados M, Nam J, Ramiro S, Voshaar M, van Vollenhoven R, Aletaha D, Aringer M, Boers M, Buckley CD, Buttgereit F, Bykerk V, Cardiel M, Combe B, Cutolo M, van Eijk-Hustings Y, Emery P, Finckh A, Gabay C, Gomez-Reino J, Gossec L, Gottenberg JE, Hazes JMW, Huizinga T, Jani M, Karateev D, Kouloumas M, Kvien T, Li Z, Mariette X, McInnes I, Mysler E, Nash P, Pavelka K, Poór G, Richez C, van Riel P, Rubbert-Roth A, Saag K, da Silva J, Stamm T, Takeuchi T, Westhovens R, de Wit M, van der Heijde D. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2016 update. Ann Rheum Dis. 2017 Jun;76(6):960-977.
- Caporali R, Crepaldi G, Codullo V, Benaglio F, Monti S, Todoerti M, Montecucco C. 20 years of experience with tumour necrosis factor inhibitors: what have we learned? Rheumatology (Oxford). 2018 Oct 1 ;57 :7.
- England BR, Smith BJ, Baker NA, Barton JL, Oatis CA, Guyatt G, Anandarajah A, Carandang K, Chan KK, Constien D, Davidson E, Dodge CV, Bemis-Dougherty A, Everett S, Fisher N, Fraenkel L, Goodman SM, Lewis J, Menzies V, Moreland LW, Navarro-Millan I, Patterson S, Phillips LR, Shah N, Singh N, White D, AlHeresh R, Barbour KE, Bye T, Guglielmo D, Haberman R, Johnson T, Kleiner A, Lane CY, Li LC, Master H, Pinto D, Poole JL, Steinbarger K, Sztubinski D, Thoma L, Tsaltskan V, Turgunbaev M, Wells C, Turner AS, Treadwell JR. 2022 American College of Rheumatology Guideline for Exercise, Rehabilitation, Diet, and Additional Integrative Interventions for Rheumatoid Arthritis. Arthritis Care Res 2023 ;75 :1603-15.


















